Metabolic Syndrome(メタボリック症候群)とは、1980年代にStanford大学のGerald M. Reavenが提唱した一群の疾病症状のことで、最初は(Metabolic) Syndrome X と呼ばれたが、後にMetabolic Syndromeと統一的に呼ばれるようになった。もともと複合的な症状を全体として把握する概念であるから、単純明快な定義があるわけではないが、予防医学的に便利な概念として、広く使われるようになった用語である。実際、Reaven以外にも、N. M. Kaplangが死の四重奏deadly quartet、R. A. DeFronzoがインシュリン抵抗性症候群syndrome of insulin resistance, 我が国のY. Matsuszawa(松澤佑次)が内臓脂肪症候群visceral fat syndromeという、類似の複合症候群の概念を提唱していた。現在のMetabolic Syndromeは、それらの流れが統合された概念である。したがって、定義にしても、診断基準にしても、厳密には統一されていない。
便宜的に言えばMetabolic Syndromeは、肥満やインシュリン抵抗性が見られ、さらに耐糖能異常gulucose intolerance、高脂血症(脂質異常、高トリグリセリド血症と低HDLコレステロール血症)、高血圧などの症状を伴う状態を意味する。疾患という概念では、肥満、2型糖尿病、高血圧、高脂血症、動脈硬化などと最も関係が深い。とくに最近では、動脈硬化性心血管疾患Atherosclerotic cardiovascular disease(ASVD)へのリスクを具現している最重要な要因と捉えるようになってきている。
Metabolic Syndromeがリスク要因となる疾患群は、かつては成人に至って多く発症するという意味で、成人病と呼ばれていた疾患群である。その後、成人病は生活習慣病と呼ばれるようになった。我々がNuclear Receptors & Syndrome X(NR-SX)計画を構想した2003年頃は、Metabolic Syndrome、メタボリック症候群という言葉はまだ十分普及していなかった。そこでSyndrome X(現在のMetabolic Syndrome)と、それに対応する日本語を生活習慣病とした。なお、Syndrome Xという用語は、循環器疾患領域ですでに別な内容(冠動脈狭窄のない虚血性心疾患という意味)で使われているため、Metabolic Syndromeが使われるようなってきた。Metabolic Syndromeについても、それをそのままカタカナ表記すればメタボリックシンドロームであるが、現在は、その半分を日本語の用語に対応させるメタボリック症候群がより使われるようになってきているので、我々もそれにしたがっている。言葉は生き物であり、時代とともに変化することは、学術用語においても同じである。
| ・ | G.M. Reaven, Banting lecture Role of insulin resistance in human disease, Diabetes, 37(12):1595-1607. 1988. |
| ・ | G.M. Reaven, Role of insulin resistance in human disease (syndrome X): an expanded definition, Annu Rev Med. 44:121-131, 1993. |
| ・ | N. M. Kaplan. The deadly quartet. Upper-body obesity, glucose intolerance, hypertriglyceridemia, and hypertension. Arch Intern Med. 149: 1514-1520, 1989; |
| ・ | R.A. DeFronzo, E. FerranniniInsulin resistance: a multifaceted syndrome responsible for NIDDM, obesity, hypertension, dyslipidemia, and atherosclerotic cardiovascular disease. Diabetes Care. 14: 173-194, 1991. |
| ・ | Y. Matsuzawa, Pathophysiology and molecular mechanisms of visceral fat syndrome: the Japanese experience. Diabetes Metab Rev. Mar;13(1):3-13, 1997. |
| ・ | T. Kaminuma, CBI Journal, 3, 130-156 , 2003 http://www.cbi.or.jp/cbi/CBIj/vol3/3_130-E.pdf |
先に注意したように、Metabolic Syndromeの定義、診断基準は国や機関で多少異なっている。世界保健機構WHOは、1999年に専門家の作業報告書を出した。米国のthe National Cholesterol Education Program (NCEP)も専門家による検討を行っている。また、米国の心臓病学会も報告書を出している。欧州も同様な作業を行っている(Liberopoulos05)。
そうした状況はLiberopoulos05とGrundy06に要領よくまとめられている。また、今日の状況については、例えばAlberti08に論じられている。
| ・ |
World Health Organization, Definition, diagnosis and classification of
diabetes mellitus and its complications. Geneva: WHO, 1999. http://www.diabetes.com.au/pdf/who_report.pdf |
| ・ | *Expert Panel on Detection, Evaluation, and Treatment of High Blood Cholesterol in Adults. Executive Summary of the Third Report of the National Cholesterol Education Program (NCEP) Expert Panel on Detection, Evaluation, and Treatment of High Blood Cholesterol in Adults (Adult Treatment Panel III). JAMA. 285: 2486-2497, 2001. |
| ・ |
*Scott M. Grundy et al., Definition of Metabolic Syndrome (Report of the National Heart, Lung, and Blood Institute/American Heart Association Conference on Scientific Issues Related to Definition), Circulation. 2004;109:433-438. http://circ.ahajournals.org/cgi/content/full/109/3/433 |
| ・ | **K. Alberti, P. Zimmet, J. Shaw, The metabolic syndrome-a new worldwide definition, The Lancet, 366(9491): 1059-1062, 2005. |
| ・ | P Zimmet et al., The Metabolic Syndrome: A Global Public Health Problem and A New Definition, Journal of atherosclerosis and thrombosis, 295-300、2005. |
| ・ | E.N. Liberopoulos, M. S. Elisaf, Diagnosis of the Metabolic Syndrome: Which Definition Should We Use?, Hellenic Journal of Cardiology, 46: 258-262, 2005. |
| ・ | S. M. Grundy, Metabolic Syndrome: Connecting and Reconciling Cardiovascular and Diabetes Worlds, Am Coll Cardiol, 47:1093-1100, 2006. http://content.onlinejacc.org/cgi/reprint/47/6/1093 |
| ・ | K G M M Alberti, P Z Zimmet,、Should we dump the metabolic syndrome? No,
BMJ336(7645):640-641, 2008. http://www.bmj.com/cgi/reprint/336/7645/641 |
日本では、松澤佑次を委員長とする日本の医学会横断的なメタボリックシンドローム診断基準検討委員会が、2004年4月に組織され、会合が重ねられて同年末には、我が国としての基準がまとめられた(内科学会雑誌05)。我が国の厚生労働省は、これを受けて検討会をもち、本年(平成20年、2008年)4月より特定健康診査・特定保健指導制度(指針)を発足させた。
| ・ | メタボリックシンドローム診断基準検討委員会、メタボリックシンドロームの定義と診断基準、日本内科学会雑誌、94(4): 794-809, 2005. |
厚生労働省検討会資料、http://www.mhlw.go.jp/shingi/2005/08/s0826-9d.html。
厚生労働省制度の資料、
http://www.mhlw.go.jp/bunya/shakaihosho/iryouseido01/info02a.html。
言葉とその内容自体少しずつ変化してきたMetabolic Syndromeであるが、専門家の間での議論も解消されたわけではない。繰り返しになるが、Metabolic Syndromeはもともと臨床医学の研究者が、病態や予防(リスク)の観点から提唱した概念である。現代医学は分子生物学を基礎とする。その分子生物学は、ゲノム技術の進歩で進歩が加速しており、その進歩は、医学の概念の見直しや、実践Practiceの見直し、予防概念の見直し、さらには教科書の書き直しを迫っている。このことはMetabolic Syndromeに関しても例外ではない。むしろ、そうした分子生物学の急激な発展によって、Metabolic Syndromeの根底にある生物の物質やエネルギー代謝のメカニズムや、化学的な分子防御機構や、脳(中枢神経系)における生理学的な統合機能、疾病に関わる分子経路網などが、急速に明らかにされてきているのが現状である。
このことから言えば、現在のMetabolic Syndromeに関する臨床で使われる定義、あるいは予防対策のための定義が、実践上の便宜を優先した大まかな指標であるように見えるのは当然のことである。それらの概念や指標は、基礎的な研究が進み、また実践を重ねることによってより適切なものに修正されていくであろうことは、言を待たないであろう。
以下は、比較的最近の総説である。
| ・ |
*I. Caroline Mcmillen and Jeffrey S. Robinson, Developmental Origins of the Metabolic Syndrome: Prediction, Plasticity, and Programming, Physiol Rev, 85:571-633, 2005. http://physrev.physiology.org/cgi/content/full/85/2/571#BIBL |
| ・ | 特集号、Metabolic Syndrome, Nature Medicine 12: 26-80, 2006. |
| ・ |
S. M. Grundy, Metabolic Syndrome: A Multiplex Cardiovascular Risk Factor, J. Clin. Endocrinol. Metab., February 1, 2007; 92(2): 399 - 404. http://jcem.endojournals.org/cgi/content/full/92/2/399 |
| ・ | *Lionel H. Opie, Metabolic Syndrome, Circulation. 2007;115:e32-e35. http://circ.ahajournals.org/cgi/content/full/115/3/e32 |
| ・ | **R. Kahn, Metabolic Syndrome: Is It a Syndrome? Does It Matter, Circulation,115: 1806-1811, 2007. |
| ・ |
**J. Jeppesen, T. W. Hansen, S. Rasmussen, H. Ibsen, C. Torp-Pedersen, and S. Madsbad, Insulin Resistance, the Metabolic Syndrome, and Risk of Incident Cardiovascular Disease: A Population-Based Study, J. Am. Coll. Cardiol., May 29, 2007; 49(21): 2112 - 2119. http://content.onlinejacc.org/cgi/content/full/49/21/2112 |
| ・ | *Christoph Schindler, Review: The metabolic syndrome as an endocrine disease: is there an effective pharmacotherapeutic strategy optimally targeting the pathogenesis?, Therapeutic Advances in Cardiovascular Disease, Vol. 1, No. 1, 7-26 (2007). |
| ・ | E. A. Ezquerra, J. M. C.Vazquez, A. A. Barrero, Obesity, Metabolic Syndrome and Diabetes: Cardiovascular Implications and Therapy, Rev Esp Cardiol, 61: 752 - 764, 2008. |
Natureの2006年の特集号は、現在のMetabolic Syndromeを概観するのに便利である。また、最後の論文(Ezquerra08)は最近のわかりやすい解説である。
2.2 Metabolic Syndromeの分子機序
我々のNR-MS計画の最終目標の一つは、Metabolic Syndromeとその関連疾患を分子経路網から理解し、医薬品開発に適した標的の探索を支援することである。この視点からとくに重要と思われる課題を以下に列挙してみる。
(1)生体における物質代謝とエネルギー変換の均衡に関わる分子機構
(2)核内受容体を中核とした脂質代謝と脂質信号の分子機構
(3)内臓脂肪細胞の役割と肥大化の分子機構
(4)肥満とインシュリン抵抗性および2型糖尿病とを関連させる分子機構
(5)脳における摂食制御の分子機構
(6)Metabolic Syndromeをリスク要因とする疾患とそれらの連関
もちろん、これらの課題は相互に関係しているから、研究論文をこれによって分類することは難しいが、現状の課題を概観するために、以下では敢えてこの分類にしたがって現状を整理してみる。
2.3 生体における物質代謝とエネルギー変換の均衡に関わる分子機構
Metabolic Syndromeの起源となる症候は、肥満であるが、肥満に限らずMetabolic Syndromeは、ヒトが食物として摂取した外界からの物質が、適切に使われず、何らかのかたちで内部に蓄積されたものと考えられる。それらの物質として主なものは、糖glucoseのような炭水化物carbohydratesと脂質lipidsである。それらの物質を変換(代謝)することで、生存に必要な生化学的な反応を推進するためのエネルギーを獲得する。このような過程は、機械が燃料を燃やして動力を発生させるのに例えられる。また「エネルギーを獲得する」とは、さまざま生化学反応で使われる万能燃料であるATPを産生する過程である。摂取する食物に較べてATPの産生や、その消費とそれに伴って産生され、体外に排出される物質が少なければ、物質の総量の収支は黒字になり、体内に蓄積されてしまう。
一般に生化学反応は、熱力学的に見て極めて効率のよい過程であるから、各反応は、それぞれの反応における(自由)エネルギーの差が少なくてすむように、複雑に絡み合っているように見える。それが生体の複雑な物質代謝系であるが、その収支を単純化すると、上のような図式となる。問題は、肥満という単純な指標の裏に隠された複雑な生理学的な代謝の仕組みであり、その病理である。その詳細が理解できなくとも、この病理過程が生体の物質とエネルギー代謝に関係していることは、容易に想像がつく。生体の物質代謝は、同化作用catabolismと異化作用anabolismに大別され、それに関わっている主な臓器は、腸と肝臓である。生体におけるエネルギー代謝とくにATP産生は、ミトコンドリアでなされる。したがって、ミトコンドリアにおけるATP産生に関わる過程が、Metabolic Syndromeという病態Pathologyに関連していることは容易に推察されるし、それを裏付ける報告は多い。
2.3.1 Mitochondoria
ヒトが呼吸で取り込む酸素のほとんどはミトコンドリアに運ばれる。ミトコンドリアは、この酸素を使って食物として取り込んだ栄養素を、最終的には水と炭酸ガスに変換し、この変換過程で生命を維持するのに必要なエネルギー(ATP)を産生する。ATPの産生は、ミトコンドリアのTCA回路cycle(クエン酸回路、Krebs 回路とも呼ばれる)と酸化的リン酸化oxidative phosphorylation (OXPHOS)によって行われる。短距離走のような呼吸が間に合わないエネルギー需要には、解糖系でATPを合成するという、無呼吸(無酸素)過程が対応する。ミトコンドリアで使われる酸素のうち数パーセントは活性酸素種Reactive Oxygen Species (ROS)に変換され、組織の損傷をもたらす。これが加齢と関係していると考えられている。このようにミトコンドリアは、生体内の生化学反応に必要なエネルギー(ATP)を供給する源であり、
ミトコンドリアのエネルギー代謝機能不全は、メタボリック症候群だけでなく、がんやアルツハイマー疾患のような神経変性症など、加齢に伴う疾患の原因となっていると考えられている(Wallace05、香川06)。
| ・ | **Science Special Issue, 5 March 1999 Vol 283, Issue 5407, Pages 1405-1592 |
| ・ | *R. A. Butow1, and N. G. Avadhani, Mitochondrial Signaling: The Retrograde Response, Molecular Cell, 14: 1-15, 2004. |
| ・ | D. C. Wallace, A MITOCHONDRIAL PARADIGM OF METABOLIC AND DEGENERATIVE DISEASES, AGING, AND CANCER: A Dawn for Evolutionary Medicine, Annual Review of Genetics. 39: 359-407, 2005. |
| ・ |
*Heidi M. McBride, Margaret Neuspiel and Sylwia Wasiak, Mitochondria: More Than Just a Powerhouse, Current Biology, Current Biology, Volume 16, Issue 14, Pages R551-R560, 2006 http://www.sciencedirect.com/science?_ob=ArticleURL&_udi=B6VRT-4KGGHGR-M&_user =10&_coverDate=07%2F25%2F2006&_rdoc=1&_fmt=&_orig=search&_sort=d&view=c&_acct =C000050221&_version=1&_urlVersion=0&_userid=10&md5= 8123cccfd4fe02db169dc3501874a1d5 |
| ・ | *Wolfgang F. Graier, Maud Frieden and Roland Malli, Mitochondria and Ca2+
signaling: old guests, new functions, Pflugers Archiv European Journal
of Physiology, 2007. DOI 10.1007/s00424-007-0296-1 http://www.springerlink.com/content/l637v84776487258/fulltext.html |
| ・ | A. Wiederkehr, C. B. Wollheim, Minireview: Implication of Mitochondria in Insulin Secretion and Action, Endocrinology 147(6): 2643-2649, 2006. |
| ・ | *L J A M. Jacobs, et al., The transmission of OXPHOS disease and methods
to prevent this, Human reproduction update, 12 (2): 119-136, 2006. http://humupd.oxfordjournals.org/cgi/content/full/12/2/119 |
| ・ | **Cecilia Saccone, Cecilia Lanave and Anna De Grassi, Metazoan OXPHOS gene families: Evolutionary forces at the level of mitochondrial and nuclear genomes, Biochimica et Biophysica Acta (BBA) - Bioenergetics, Volume 1757, 2006. |
| ・ | Jeffrey S Armstrong, Mitochondria: a target for cancer therapy, British Journal of Pharmacology 147, 239-248, 2006. |
| ・ | 香川靖雄、ミトコンドリアのエネルギー代謝と健康、体力科学、55: 175-180. 2006. |

2.3.2 AMPK Pathway
AMP-activated protein kinase (AMPK)は、エネルギーの需要の計りであり、AMP/APTの値が上昇すると、AMPKが活性化され、筋肉における脂肪酸の取り込みや、糖の輸送や分解が促進される。こうしたAMPK経路の機能不全もメタボリック症候群の原因になると考えられている。
| ・ | *L.G.D. Fryer and D. Carling, AMP-activated protein kinase and the metabolic syndrome, Biochem. Soc. Trans. 33: 362-366, 2005. |
| ・ | *Richard M. Reznick and Gerald I. Shulman, The role of AMP-activated protein kinase in mitochondrial biogenesis, J. Physiol. 574(1): 33-39, 2006. |
| ・ | M. Arad, C. E. Seidman, J.G. Seidman, AMP-Activated Protein Kinase in the Heart: Role During Health and Disease, Circulation Research, 100:474-488, 2007 |
2.3.3 UCP superfamily
UCP1, UCP2, UCP3は、ミトコンドリアの内膜に存在し、Superfamily を構成するanion carrier proteinである。このうちUCP1は遺伝子がクローニングされる前から、褐色脂肪細胞に存在し、ATP産生に依存することなく、ミトコンドリアの内膜の水素イオンH+の電気化学的な電位勾配を消滅させることで発熱を促すと同時にエネルギー効率を減少させるという機能が知られていた。UCP2、UCP3は遺伝子としての配列から見つかれたものである。UCP2の変異が糖尿病で見つかったことから、これらのSuperfamilyのMetabolic Syndromeへの関与が疑われている(Fisler06)。現在Superfamilyには、UCP4、UCP5も追加されている。
| ・ | L. T. Dalgaard and O. Pedersen, Uncoupling proteins: functional characteristics and role in the pathogenesis of obesity and Type II diabetes, Diabetologia, 44(8): 946-965, 2001 |
| ・ |
Janis S Fisler and Craig H Warden, Uncoupling proteins, dietary fat and the metabolic syndrome, Nutrition & Metabolism 3:38, 2006. http://www.nutritionandmetabolism.com/content/3/1/38 |
| ・ | **Yi-Hsiang Hsu et al., Gnetic Variants in the UCP2-UCP3 Gene Cluster and Risk of Diabetes in the Women's Health Initiative Observational Study, Diabetes 57:1101-1107, 2008 |
2.4 糖および脂質の代謝と信号伝達の分子機構
核反応を伴わない生体反応においては、生体が必要とするエネルギーを賄うのは、物質の代謝である。この意味でエネルギー代謝は、物質代謝と独立には考えられない。そしてエネルギー代謝に随伴する物質代謝は糖(炭水化物)あるいは脂肪の代謝である。
このうち糖の代謝を調節するホルモンがインシュリンInsulinである。しかもインシュリンは、そうした役割を担っている生体内の唯一の調節物質(ペプチド)である。したがってこの物質の過不足や機能不全が直接、糖尿病のような疾患に結びつくことになる。糖質代謝に関わるヒトのこの特徴は、昔から知られていたことであるが、脂質に関わる代謝が解明されてきたのは比較的最近のことである。とくに脂質に関わる代謝とMetabolic Syndromeの関連が指摘され始めたのは、核内受容体のうちのOrphan Receptor の役割が解明されてきたことによる(Chawla01)。ここでの代謝は、単なる酵素反応過程ではなく、核内受容体やその類縁の転写因子であるSREBP, C/EBPなどを介した、遺伝子発現を伴った過程である(Desvergne06)。これは、核内受容体とMetabolic Syndromeを結ぶ中核となる過程である。なお、2008年のNature Review Molecular Cell Biologyの2月号には、脂質の健康と病態に関する研究が特集されている。
| ・ | *Ajay Chawla, Joyce J. Repa, Ronald M. Evans, David J. Mangelsdorf, Nuclear Receptors and Lipid Physiology: Opening the X-Files, SCIENCE, VOL 294: 1866-1870, 2001. |
| ・ |
*Beatrice Desvergne, Liliane Michalik and Walter Wahli, Transcriptional Regulation of Metabolism, Physiol. Rev. 86: 465-514, 2006; (http://physrev.physiology.org/cgi/reprint/86/2/465) |
| ・ | *Vincent Poitout, β-Cell Lipotoxicity: Burning Fat into Heat?, Endocrinology 145(8):3563-3565, 2004. |
| ・ | *Alistair VW Nunn, Jimmy Bell and Philip Barter, The integration of lipid-sensing and anti-inflammatory effects: how the PPARs play a role in metabolic balance, Nucl Recept. 2007; 5: 1. http://www.pubmedcentral.nih.gov/articlerender.fcgi?artid=1899481 |
| ・ | M. P. Wymann, R. Schneiter, Lipid Signaling in Disease, Nature Review Molecular Cell Biology, 9: 162-176, 2008. |
最近注目されているのは、物質とエネルギー代謝の中核役となる核内受容体の介添え役として機能する、転写の共役因子ではない、タンパク質である。その例としてFibroblast Growth Factor 21(FGF21)がある(Inagaki07)。FGF21は、22種類あるFGFファミリー(FGF1-23、ただしFGF15はない)に属するが、これまで知られていたFGFと異なり、PPARαと相互作用することで、代謝などに関与することが発見され、治療の標的としても期待されている(Shanafelt08)。FGF21は空腹時に脳に至る信号分子の役割も果たしているという知見も報告されており、摂食行動との関係が示唆されている。また、FGF21とPPARγとの相互作用も報告されている(Moyers07)
| ・ | A. Kharitonenkov et al., FGF-21 as a novel metabolic regulator, The Journal of Clinical Investigation, 115(6): 1627-1635, 2005 |
| ・ | **Takeshi Inagaki et al., Endocrine Regulation of the Fasting Response by PPARα-Mediated Induction of Fibroblast Growth Factor 21, Cell Metabolism, 5(6): 415-425, 2007. |
| ・ | **M. L. Reitman, FGF21: A Missing Link in the Biology of Fasting. Cell Metabolism 5(6):405-407, 2007 |
| ・ | **Hong Wang, Li Qiang, and Stephen R. Farmer, Identification of a Domain within Peroxisome Proliferator-Activated ReceptorγRegulating Expression of a Group of Genes Containing Fibroblast Growth Factor 21 That Are Selectively Repressed by SIRT1 in Adipocytes、Molecular and Cellular Biology, 28(1): 188-200, 2008. |
| ・ | J. S. Moyers et al,, Molecular Determinants of FGF-21 Activity-Synergy and Cross-Talk With PPARg Signaling, JOURNAL OF CELLULAR PHYSIOLOGY 210:1-6, 2007. |
| ・ | **A. Kharitonenkov et al., Fibroblast Growth Factor-21 as a Therapeutic Agent for Metabolic Diseases. Novel Therapeutic Strategies , Biodrugs. 22(1):37-44, 2008. |
FGF23については、老化に関わる遺伝子として発見されたα-Kloth、およびそのホモログであるβ-Kloth、および膜輸送タンパク質 Na+,K+-ATPase、さらにビタミンD受容体などが複雑に関わったカルシウムの恒常性に関係しいるとされている(Kuro-o06)。
| ・ | E. Tomlinson et al., Transgenic mice expressing human fibroblast growth factor-19 display increased metabolic rate and decreased adiposity. Endocrinology, 143:1741-1747, 2002. |
| ・ | L. Fu, et al., Fibroblast growth factor 19 increases metabolic rate and reverses dietary and leptin deficient diabetes. Endocrinology. 145:2594-2603, 2004. |
| ・ | Alison M. Strack and Robert W. Myers, Modulation of Metabolic Syndrome by Fibroblast Growth Factor 19 (FGF19)?, Endocrinology Vol. 145, No. 6 2591-2593, 2004 |
| ・ | M. Kuro-o, , Klotho as a regulator of fibroblast growth factor signaling and phosphate/calcium metabolism. Renal pathophysiology, Current Opinion in Nephrology & Hypertension. 15(4):437-441, 2006. |
| ・ | M. Emmett, What does serum fibroblast growth factor 23 do in hemodialysis patients?, Kidney International 73, 3-5: 2008. |
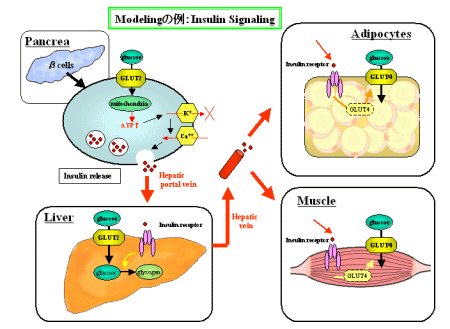
糖および脂質の代謝と信号伝達の分子機構を解明することの難しさは、腸、肝臓、腎臓、さらに脂肪組織というような関係する各種の臓器や組織の中の個々の細胞における転写を介した代謝過程だけでなく、それらの臓器からの分泌物が長距離輸送され、他の臓器に影響を及ぼす過程が関わっているからである。とくに分子生物学の問題ではなく、臨床医学の立場からすると、こうした全身的systemicな制御系を解析する必要があるが、このことは、培養細胞をもちいた発現解析などより、桁違いに難しい仕事である。こうした仕事には、例えば胆汁酸Bile Acidの役割の解明なども含まれる。
| ・ | S. M. Houten, J. Auwerx, The enterohepatic nuclear receptors are major regulators of the enterohepatic circulation of bile salts. Ann. Med., 36: 482-491, 2004. |
| ・ | C. Thomas et al., Targeting the bile-acid signaling for metabolic diseases, Nature Reviews Drug Discovery, 7: 678-693, 2008. |
2.5 肥満の分子機構、および内臓脂肪細胞の役割と肥大化の分子機構
内臓脂肪組織 Visceral Adipose Tissue
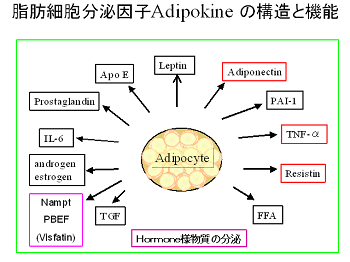
Metabolic Syndromeの2つの特徴、肥満とインシュリン抵抗性のうち、生活習慣病へのリスクを高める肥満の原因が皮下脂肪ではなく内臓脂肪であることが、当時大阪大学にいた松澤祐次らがCTスキャナーなどを使った診断データにより提唱された。Metabolic Syndromeの源流を内臓脂肪組織Visceral Adipose Tissueの肥大化とするこの考えは、現在、広く受け入れられており、(内臓)脂肪細胞Adipocyteの研究は、Metabolic Syndrome研究の基盤とも言える位置を占めている。そうした研究課題は多岐にわたるが、ざっと概観しただけでも、白色脂肪細胞White Adipose Tissueである内臓脂肪組織と褐色脂肪組織Brown Adipose Tissueの違い、脂肪細胞の形成Adipogeneis, 脂肪細胞が分泌する多彩な因子Adipokinesの構造と機能と組織特異性、脂肪組織が原因となる炎症Inflammationとそれに関係したAdipokinesとマクロファージMacrophageの役割、Adipokinesの他組織あるいは全身的systemeicな影響解析、などが挙げられる。Adipokinesとしては、糖尿病と関係の深いAdiponectine、肥満と関係したleptinやresistin、炎症と関係したTNF-βやIL-6, Sirtuinと関係したVisfatin(Nampt, PBEF)、さらに脂肪酸FFA、PAI-1, ApoE, Estrogen, Androgen, Prostaglandin, TGFなどが知られているが、その全貌はまだ解明されていない。
個体全体から見た脂肪組織の役割は、エネルギーの収支バランスの調節と、糖Glucoseの恒常性の維持であるが、現在、病態生理学Pathphysiology的な立場から関心が集まっているのが、炎症Inflammationとの関係である。炎症はがん化につながるから、これは肥満とがんを結ぶ経路を示唆している。
| ・ | **Y. Matsuzawa, T. Funahashi, T, Nakamura, Molecular mechanism of metabolic syndrome X: contribution of adipocytokines adipocyte-derived bioactive substances, Annals of the New York Academy of Sciences, 892:146-154, 1999. |
| ・ | *Bernardo Leo Wajchenberg, Subcutaneous and Visceral Adipose Tissue: Their Relation to the Metabolic Syndrome, Endocrine Reviews 21 (6): 697-738, 2000. |
| ・ | Michael W. Rajala and Philipp E. Scherer, Minireview: The Adipocyte-At the Crossroads of Energy Homeostasis, Inflammation, and Atherosclerosis, Endocrinology Vol. 144, No. 9 3765-3773, 2003. |
| ・ | Stuart P. Weisberg et al., Obesity is associated with macrophage accumulation in adipose tissue, J Clin Invest. 112(12): 1796-1808, 2003. |
| ・ | E. S. Freedland, Role of a critical visceral adipose tissue threshhold (CVATT)in metabolic syndrome: implication for controllingdietry carbohydrate: a review, Nutrition & Metabolism, 1(12), 2004 |
| ・ | A. H. Berg, P. E. Scherer, Adiose Tissue, Inflammation, and Cardiovasucular Disease, 96: 939-949, 2005 |
| ・ | G. Hotamisligil, Inflammation and Metabolic Syndrome, 444: 860-867, 2006. |
| ・ | E. Rosen, S. B. Spiegelman, Adipocytes as regulators of energy balance and glucose homeostasis, Nature, 444: 847-853, 2006. |
| ・ | J. K. Sethi, A. J. Vidal-Puing, Adipose tissue function and plasticity orchestrate nutritional adaptation, Journal of Lipid Research, 48: 1253-1262, 2007. |
| ・ | *Silvia I Anghel and Walter Wahli, Fat poetry: a kingdom for PPARγ, Cell Research 17:486-511, 2007. |
| ・ | Ram Weiss, Fat distribution and storage: how much, where, and how?, European Journal of Endocrinology, 157(suppl_1): 39-45, 2007. |
脂肪細胞の形成 Adipogenesis
核内受容体との関係で言えば、脂肪細胞の形成にPPARγと類縁の転写因子C/EBPαやC/EBPβなどが関与していることであるが、これ以外の転写因子、例えばKLF5その他の関与も報告されている(Oishi05, Farmer06、Rosen06)。脂肪細胞の由来についてはよくわかっていなかったが、最近、褐色脂肪細胞と白色脂肪細胞の由来が解明され始めた。それによれば、胚幹細胞Embryonic Stem cellから、間充織幹細胞Meshenchymal stem cellへと分化してきた細胞が、転写因子の働きの違いにより、一方では筋肉や褐色脂肪細胞に分化し、他方では白色細胞の分化するという知見が報告されている。この分化にはBMP(Bone Morphogenic Protein)-7などの転写因子が関与している。褐色脂肪細胞が、脂肪細胞と筋肉細胞の双方の性質を併せもっていることは古くから指摘されていたが、このことは、提唱された細胞系譜からも推測されることである(Tseng08、Seale 08)。
| ・ | Y. Oishi et al., Kruppel-like transcription factor KLF5 is a key regulator of adipocyte differentiation, Cell Metabolism, 1: 27-39, 2005. |
| ・ | S. R.Farmer, Transcriptional control of adipocyte formation. Cell Metab. 4, 263-273, 2006. |
| ・ | **E. D.Rosen, & O. A. MacDougald, Adipocyte differentiation from the inside out. Nature Rev. Mol. Cell Biol. 7: 885-896, 2006. |
| ・ | Y.-H. Tseng et al. Nature 454: 1000-1004, 2008. |
| ・ | P. Seale et al., Nature 454: 961-967, 2008. |

Adipokines
単なる脂肪というエネルギー源の蓄積だけではなく、多臓器と制御信号分子を交換する(最大の)ホルモン器官としての脂肪組織の役割を明らかにするには、脂肪組織が分泌し、また受容する信号分子を網羅的に捉えなければならない。これらの分泌因子の機能は、脂肪組織でどのように産生あるいは輸送され、その内部でどのような役割を果たしているかというだけでなく、肝臓、筋肉、脳、膵β細胞、(Macrophageのような)免疫を担う血液細胞など、他の臓器や組織にどのような影響を与えているのかをしらべてみなければ、理解できない。例えば、Adiponectineに関しては、その2種の受容体が発見され(Kadowaki06)、さらにその投与がインシュリン抵抗性を改善することが確認されている(Yamauchi01)。また、leptinについては脳における摂食制御系への信号であることがわかっており、TGF-αやIL-6については炎症と関係していること、MCP-1についてはマクロファージを脂肪組織に移行させること(Kamei06)などが知られているが、遊離脂肪酸FFAのように多彩な機能を担っているものは、研究されてはいてもまだ十分理解されているとは言えない。Adipokineの総数は、百を越えると推定されているから、その全容解明"Adiokinome"は、まだ残された課題である(Trayhurn04)。
| ・ | P. Trayhurn, L. S. Wood, Adipokines and the pleiotropic role of white adiose tissue, British Journalof Nutrition, 92: 347-355, 2004. |
| ・ | J. K. Sethi, A. J. Vidal-Puing, Adipose tissue function and plasticity orchestrate nutritional adaptation, Journal of Lipid Research, 48: 1253-1262, 2007. |
| ・ | T. Kadowaki et al., Adiponectin and adiponectin receptors in insulin resistance, diabetes, ant the metabolic syndrome, The Journal of Clinical Investigation, 116(7): 1784-1792, 2006. |
| ・ | T. Yamauchi et al., The fat-derived hormone adiponectine reverses insulin resistance associated with both lipoatrophy and obesity, Nature Medicine , 7(8): 941-946, 2001. |
| ・ | N. Kamei et al., Overexpression of Monocyte Che,pattractant Preotein-1 in AdiposeTissue Causese Macrophage Recruitement and Insulin Resistance, The Journal of Biological Hemistry, 281: 26602-26614, 2006. |
2.6 肥満とインシュリン抵抗性と2型糖尿病とを関連させる分子機構
この課題は、臨床医学から見たMetabolic Syndromeの中心的な課題の一つである。肥満とインシュリン抵抗性と2型糖尿病との因果関係は、疫学的あるいは臨床医学の経験的事実として広く認識されているが、それをつなぐ分子機構に関しては、インシュリン、Adiponectine、resistinなど、多様なAdipokineがさまざまな役を果たしているであろうと考えられているが、まだ十分にはわかっていない。
| ・ | *S. Kahn et al., Mechanisms linking obesity to insulin resistance and type 2 diabetes, Nature, 444, 840-846 , 2006 |
| ・ | J-P. Bastard et al., Recent advances in the relationship between obesity, inflammation, and insulin resistance, Eur. Cytokine Netw., 17(1): 4-12, 2006. |
| ・ |
*Kitt Falk Petersen et al., The role of skeletal muscle insulin resistance in the pathogenesis of the metabolic syndrome, PNAS, 104(31): 12587 - 12594, 2007; http://www.pnas.org/cgi/content/full/104/31/12587 |
| ・ | M. Qantanai, M. A. Lazar, Mechanisms of obesity-associated insulin resistance: many choises on the menu, Genes & Dev., 21: 1443-1455, 2007. |
| ・ | J. A. J. Martyn, M. Kaneki, S. Yasuhara, Obesity-induced Insulin Resistance and Hyperglycemia, Anesthesiology 109:137-48, 2008. |
食物を求めることは、生存するための動物の根源的な行動であり、その基盤となる分子機構が進化的に保存されているのも、当然であろう(Fitzpatrick04、Stanley05)。ヒトに関してはこれに食の文化という要素が加わる。Metabolic Syndromeとそれに関連した肥満や糖尿病改善の第1に節食が挙げられているが、食事制限による体重低下を維持することはそう易しくない。このことについては、食事を「食物への惑溺addiction」と捉え、麻薬などと同じような「依存症治療」の概念で対処するという考えがある(Volkow07)。そこでは食欲の抑制が課題であるが、この課題に分子経路網の知識からアプローチすることも少しずつ可能になってきている。実際に、治療薬として脳内の麻薬の受容体を標的とする薬も開発されている(治療標的の項参照)。
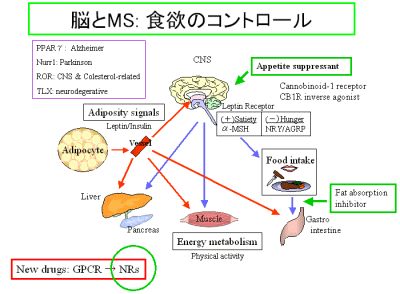
ヒトの摂食に関与する主要臓器は、脂肪組織、肝臓、腸(消化管)、そして脳である。この系の全体を統括するのは、もちろん脳である。体の中の食物の蓄積状態は、十分であれば脂肪組織や肝臓や消化管からのSatiety(満腹)信号として、不十分であれば同じ脂肪組織や肝臓および消化管からの飢餓(食欲、Food reward)信号として脳に到達する。これら2つの信号は、そこでそれぞれ摂食中止(no food intake)ないし、摂食せよ(food intake)という命令信号に変換される。脂肪組織からの信号leptinやinsulinは、視床下部のarcuate nucleus(ARC)から脳に入り、肝臓と消化管からの信号は、nucleus tractus solitarius (NTS)から脳の他の領域に伝達される。この2つの入り口からの信号は、脳の中の複雑な回路でつながれている(Schwartz00、Morton06)。
消化管からの脳への信号分子の一つがグレリンGhrelinであるが、それと一緒に働くのがneuropeptide Y (NPY)とアグーチ関連タンパク質agouti-related protein(AgRP)である。最近、視床下部にあるこのNPY/AgRP神経細胞に対するグレリンの作用が、UCP2にによって除去される、脂肪酸の酸化に関与した経路分子に依存していることが報告された(Andrews08)。
| ・ | N. D. Volkow, C. P. O'Brien, Issues for DSM-V: Should Obesity Be Included as a Brain Disorder?, Am. J. Pyschiatry, 164(5): 708-710, 2007. |
| ・ | M. J. Fitzpatrick, M. B. Sokolowski, In Search of Foods: Exploring the Evolutionary Link Between cGMP-Dependent Protein Kinase (PKG) and Behaviour, Integr. Comp. Biol., 44: 28-36, 2004. |
| ・ | Sarah Stanley et al., Hormonal Regulation of Food Intake, Physiol. Rev.
85: 1131-1158, 2005 http://physrev.physiology.org/cgi/reprint/85/4/1131 |
| ・ | M. W. Schwartz et al., Central nervous system control of food intake, Nature 404: 661-671, 2000. |
| ・ | G. J. Morton et al., Central nervous system control of food intake and body weight, Nature 443: 289-295, 2006. |
| ・ | A. Abizaid, Q. Gao and T. L. Horvath, Thoughts for Food: Review Brain Mechanisms and Peripheral Energy Balance, 51(6): 691-702, 2006. |
| ・ | K. W. Williams, R. Coppari and J.. Elmquist, "AMPing up" our understanding of the hypothalamic control of energy balance, J. Clin. Invest. 117(8): 2089-2092, 2007. http://www.jci.org/articles/view/32975 |
| ・ | M. Claret et al., AMPK is essential for energy homeostasis regulation and
glucose sensing by POMC and AgRP neurons, J. Clin. Invest. 117(8): 2325-2336,
2007. http://www.jci.org/articles/view/31516 |
| ・ | Z. B. Andrews et al., UCP2 mediates ghrelin's action on NPY/AgRP neurons by lowering free radicalsNature 454: 846-851, 2008. |
| ・ | M. Lo´pez et al., Peripheral tissue-brain interactions in the regulation of food intake, Proceedings of the Nutrition Society 66, 131-155, 2007. |
| ・ |
L. E. Parton et al., Glucose sensing by POMC neurons regulates glucose homeostasis and is impaired in obesity, Nature. 449:228-32、2007 |
| ・ | Annika Herwig et al., Hypothalamic Thyroid Hormone in Energy Balance Regulation, Onkologie 31:71-79, 2008. |
| ・ | **Eva Rother, A. Christine Konner, and Jens Bruning, Neurocircuits integrating hormone and nutrient signaling in control of glucose metabolism, Am J Physiol Endocrinol Metab (February 19, 2008). |
Metabolic Syndromeはいわゆる生活習慣病と言われるような関連疾患を発症する危険性が高い状態を意味する。これらの疾患それぞれについては、これまでも研究されてきているので、Metabolic Syndromeの視点からは、Metabolic Syndromeとくに、肥満からこれら個々の疾患にどのように移行するか、その確率(Risk)とその予防法Interventionが問題になる。こうした問題は、Metabolic Syndromeを理解するための要素的な問題と深く関連しており、事実上それらを分離するのは、極めて困難であるが、以下では便宜的に、この問題に関するこれまでふれていなかった論文を紹介する。なお、ここでの論文は、Metabolic Syndrome治療薬の標的の項の論文とも関係が深い。
Obesity
| ・ | D. E. Cummings and Pathology of Human Obesity, Ann. Rev. Med., 54: 453-471, 2003. |
| ・ | J. S. Flier, Obesity Wars: Molecular Progress Confronts an Expanding Epidemic, Cell, 116: 337-350, 2004. |
| ・ | M. Mello et al., Obesity- the New Frontiers of Public Health Law, The New England Journal of Medicine, 354(24): 2601-2610, 2006. |
Obesity-Inflammation
肥満と炎症をつなぐのは、内臓脂肪であり、そこに集まってくるマクロファージMacrophageである。炎症は免疫系を刺激し、がんにつながる症状であり、Metabolic
Syndromeが原因となる重要なリスク要因と考えられている。炎症に関しては、Naturega
2008年7月24日号のNature Insightで特集しているが、そこには核内受容体の役割やMetabolic Syndromeとの関係が解説され、小胞体ERの役割が強調されている(Zhang08、Handchin08、Bensinger08)。
| ・ | S. P. Weisberg et al., Obesity is associated with macrophage accumulation in adipose tissue, The Journal of clinical Investigation, 112(12): 1796-1808, 2003. |
| ・ | *G. S. Hotamisligi, Inflammation and metabolic disorders, Nature 444: 860-867, 2006. |
| ・ | J. I. Odegarard et al., Macrophage-specific PPARγ controls alternative activation and improves insulin resistance, Nature, 447: 1116-1120, 2007 |
| ・ | K.Zhang & R. J. Kaufman, From endoplasmic-reticulum stress to the inflammatory response, Nature, 454: 455-462, 2008 |
| ・ | C. Handschin & B. M. Spiegelman, The role of exercise and PGC1 in inflammation and chronic disease, 454: 463-469, 2008. |
| ・ | S. J. Bensinger & P. Tontonoz Integration of metabolism and inflammation by lipid-activated nuclear receptors, 454: 470-478, 2008. |

Insulin Resitance/Type 2 Diabetes
Metabolic Syndromeあるいは肥満からどのように2型糖尿病に移行するかを、分子機構から説明することはまだ十分できていない。およその流れについては例えばKahn06にある。
| ・ | M. Stumvoll, B. Goldstein, T. W. van Haeften, Type 2 diabetes: principles of pathogenesis and therapy, 365: 133-1346, 2005. |
| ・ | I. Barroso, Genetics of Type 2 diabetes, Diabetic Medicine, 22: 517-535, 2005. |
| ・ | *S. Kahn et al., Mechanisms linking obesity to insulin resistance and type 2 diabetes, Nature, 444, 840-846 , 2006 |
| ・ | Sudha B. Biddinger and C. Ronald Kahn, FROM MICE TO MEN: Insights into the Insulin Resistance Syndromes, Annual Review of Physiology Vol. 68: 123-158 (Volume publication date January 2006) |
| ・ | P. K. Shah, Innate Immune Pathway Links Obesity to Insulin Resistance, Circ. Res. 100;1531-1533, 2007. |

Hypertention
| ・ | *F Tesfaye et al., Association between body mass index and blood pressure
across three populations in Africa and Asia, Journal of Human Hypertension,
21, 28-37, 2007. http://www.nature.com/jhh/journal/v21/n1/full/1002104a.html |
| ・ | *P. Margozzini, A. Rigotti, C. Ferreccio, N. Quezada, M. Garrido, and G.
Valdes Review: Hypertension and the cardiometabolic syndrome in Chile: a review of concepts and consequences for the developing world, Therapeutic Advances in Cardiovascular Disease, February 1, 2007; 1(1): 83 - 90 |
Dyslipidemia
| ・ | Heather Basciano, Lisa Federico and Khosrow Adeli, Fructose, insulin resistance, and metabolic dyslipidemia, Nutrition & Metabolism, 2:5, 2005, |
Cardiovascular Disease
Metabolic Syndromeが最初に提唱された頃は、心血管疾患、とくに動脈硬化性の心血管疾患へ移行するリスクが大きな関心の的であった。現在でも心血管疾患は、Metabolic Syndromeの言わば終着点だと見なされている。分子機構の観点からは、脂肪細胞の炎症、それに影響されたMacrophageの循環、血管内皮細胞への影響などが、Metabolic Syndromeと心血管系の疾患とをつなぐ病態と見られている。こうした疾患の推移の見極めと適切な介在interventionは、臨床医学の課題である。
| ・ |
S. M. Grundy, Metabolic Syndrome: A Multiplex Cardiovascular Risk Factor, J. Clin. Endocrinol. Metab., 92(2): 399 - 404, 2007. http://jcem.endojournals.org/cgi/content/full/92/2/399 |
| ・ | *Toshiharu Ninomiya, Impact of Metabolic Syndrome on the Development of Cardiovascular Disease in a General Japanese Population The Hisayama Study, Stroke, July 1, 2007; 38(7): 2063 - 2069 http://stroke.ahajournals.org/cgi/content/full/38/7/2063 |
| ・ |
Donald M. Lloyd-Jones et al., Consistently Stable or Decreased Body Mass Index in Young Adulthood and Longitudinal Changes in Metabolic Syndrome Components The Coronary Artery Risk Development in Young Adults Study, Circulation. 115:1004-1011, 2007. http://circ.ahajournals.org/cgi/content/full/115/8/1004 |
神経変性症Neurodegenerative Disease
アルツハイマー疾患やパーキンソン疾患などは、神経細胞の中のある種のタンパク質が正常に折り畳まれなくなり、また神経細胞が死滅するという分子病態を呈することが知られている。このような神経変性疾患が、糖や脂質の代謝異常という点で、Metabolic Syndromeと共通性があるのではないかという考えが浮上している。神経変性症に関する研究が進めば、両者の関係も分子機構のレベルで明らかにされるであろう。実際、PPARなど核内受容体を標的とする神経変性症治療薬が開発されている(Chaturvedi08)。
| ・ | M. P. Mattson, S. L. Chan, W. Duan, Modification of Brain Aging and Neurodegenerative Disorders by Genes, Diet, and Behavior, Physiological Review, 82: 637-672, 2002. |
| ・ | **B. V. Zlokovic, New Therapeutic Targets in the Neurovascular Pathway in Alzheimer's Disease, Neurotherapeutics 5( 3): 409-414, 2008. |
| ・ | R. K. Chaturvedi and M. F. Beal, PPAR: a therapeutic target in Parkinson's disease, Journal of Neurochemistry, 106(2): 506 - 518, 2008. |
その他の疾患
糖尿病が腎疾患を併発することはよく知られているが、Metabolic Syndromeあるいは生活習慣病と関連すると考えられている疾患は、骨粗鬆症、歯周病、痛風など、いろいろある。これらについても、今後明らかにされていくだろう。骨粗鬆症は骨芽細胞Osteoblastと破骨細胞Osteoclastの働きのバランスの崩れと見なされ、治療は前者の活性化か後者の抑制ということになる。これまでは後者のBisphosphonateやエストロゲンが使われていたが、最近前者を操作する新しい薬(PYK2-Inhibitor)の可能性が報告されている (Kingsley07)。歯周病に関しては心血管疾患のリスク因子であると考えられている。通風に関しては、血液中の尿酸値の高さとMetabolic Syndromeを特徴づける内臓脂肪量とAdiponectineの減少との間に関係があることが報告されている(Tamba08)。
| ・ | E. Ritz、Metabolic Syndrome: An Emerging Threat to Renal Function, Clin J Am Soc Nephrol. 2: 869-871, 2007. http://cjasn.asnjournals.org/cgi/content/full/2/5/869 |
| ・ | L. A. Kingsley, J. M. Chirgwin, T. A. Gruise, Breaking new ground to build bone, PNAS, 104(26): 10753-10754, 2007. |
| ・ | H. Choi et al, Prevalence of the Metabolic Syndrome in Patients With Gout: The Third National Health and Nutrition Examination Survey, Arthritis & Rheumatism (Arthritis Care & Research), 57 (1): 109-115, 2007. |
| ・ | **J.G. Puig, M. A. Martinez, Hyperuricemia, gout and the metabolic syndrome. Crystal deposition diseases, Current Opinion in Rheumatology. 20(2):187-191, 2008. |
| ・ | S. Tamba et al., Relationship between the Serum Uric Acid Level, Visceral Fat Accumulation and Serum Adiponectin Concentration in Japanese Men, Inter. Med., 47: 1175-1180, 2008 |
Aging
最近Agingの研究が盛んになってきた。その契機となったのは、単一の遺伝子の変異が寿命を延ばすことが線虫で発見されたことである(Klass98、Friedman88)。その後、食事制限(Dietary restriction、Calorie Restriction)によって寿命が延びることが酵母、線虫、ショウジョウバエ、マウスなどのモデル系で見つかり、寿命に関わる共通分子としてSirtuinが、また共通経路としてはInsulin Signalの経路(IIS Pathway)が発見された(Kenyon05)。現在では、TOR Pathwayやミトコンドリア経路も寿命に関係した経路であると考えられている(Greer08)。
Metabolic SyndromeとAgingとの関係は、Agingの根底に代謝経路網metabolic pathway/networkの変化があることから、当然、深い関係があること推察されるが、最近は双方の研究で問題にされる遺伝子、タンパク質、経路網の重複が顕著になってきている。
一方Agingの観点からは、ミトコンドリアで産生される活性酸素種ROSとの関係、その消去にかかわるNrf2などの関与が指摘されている。これは、ATP産生に伴って発生するROSが適切に処理されることが長寿につながるという概念であるが、活性酸素を直接消去する酵素だけでなく、活性酸素ストレスを受けた転写を介した処理酵素の産生が重要という視点も浮上している。
いずれにしてもAgingは、極めて複雑な過程であり、簡便なモデル動物による解析は、ヒトの長寿機構解明のヒントを与えるものであるが、明快な答えを与えるものではない(Andrews08、Kirkwood08)。
| ・ | Klass, M. R. A method for the isolation of longevity mutants in the nematode Caenorhabditis elegans and initial results. Mech. Ageing Dev. 22, 279-286, 1983. |
| ・ | Friedman, D. B. & Johnson, T. E. A mutation in the age-1 gene in Caenorhabditis elegans lengthens life and reduces hermaphrodite fertility. Genetics 118, 75-86, 1988 |
| ・ | Kenyon, C. The plasticity of aging: insights from long-lived mutants. Cell 120, 449-460, 2005. |
| ・ | R. Curtis, B. J. Geesaman and P. S. DiStefano , AGEING AND METABOLISM: DRUG DISCOVERY OPPORTUNITIES, Nature Reviews Drug Discovery 4, 569-580 (2005) |
| ・ | *Masaya Yamamoto et al., Regulation of Oxidative Stress by the Anti-aging Hormone Klotho, J. Biol. Chem., Vol. 280, Issue 45, 38029-38034, November 11, 2005. |
| ・ | *Toren Finkel Manuel Serrano & Maria A. Blasco, The common biology
of cancer and ageing, Nature 448:767-774, 2007. http://www.nature.com/nature/journal/v448/n7155/full/nature05985.html |
| ・ | E. L. Greer and A. Brunet, Signaling networks in aging, Journal of Cell Science, 121(4): 407-412, 2008. |
| ・ | Jan Vijg & Judith Campisi, Puzzles, promises and a cure for ageing, Nature 454, 1065-1071, 2008. |
| ・ | Thomas B. L. Kirkwood, A systematic look at an old problem, Nature 451, 644-647, 2008. |

(Jan Vijg & Judith Campisi, Puzzles, promises and a cure for ageing, Nature 454, 1065-1071, 2008のFig. 1)
NAD-Sirtuin-PGC1 Axis
線虫から始まったAging研究からの流れで関心が集まっているのがNAD, Sirtuin、PGC1という生体分子群である。Sirtuin(Sir2ファミリー)への関心は、酵母、線虫、ショウジョウバエ、マウスまで、カロリー制限をした生物の寿命が延びるという観察に端を発している。線虫、ショウジョウバエ、マウスの寿命に関わる経路がInsulin/IGFからの信号経路であるのに対し、酵母ではSirtuinあるいはSirと呼ばれる、NAD依存性の脱アセチル化酵素活性をもつタンパク質ファミリーが関与していることが見出された(Imai00)。このファミリーに属するSir2は、線虫やショウジョウバエでも存在し、さらに類似のタンパク質ファミリーはヒトでも見つかっている。Imai(今井眞一郎)は、、NADは全身をめぐる血液中にNADが存在することは、NAD合成系が全身的な制御に関与していることを示唆しており、臨床的に極めて重要だと指摘している。現在、SirtはPPARγの共役因子であるPGC1と相互作用することも知られており、NAD-Sirtuin-PGC1という分子経路が、寿命、Metabolic Syndrome さらにはがん化などに関与していると指摘されている。
| ・ | Shin-ichiro Imai et al., Transcriptional silencing and longevity protein Sir2 is an NAD-dependent histone deacetylase, Nature 403, 795-800、2000. |
| ・ | *Javier R. Revollo, Andrew A. Grimm, and Shin-ichiro Imai, The NAD Biosynthesis Pathway Mediated by Nicotinamide Phosphoribosyltransferase Regulates Sir2 Activity in Mammalian Cells, THE JOURNAL OF BIOLOGICAL CHEMISTRY Vol. 279, No. 49, Issue of December 3, pp. 50754-50763, 2004 |
| ・ | *Leonard Guarente and Frederic Picard, Calorie Restriction-the SIR2 Connection, Cell, 120: 473-482, 2005, |
| ・ | *Alexander Bu¨ rkle, Poly(ADP-ribose) The most elaborate metabolite of NAD+, FEBS Journal 272; 4576-4589, 2005 |
| ・ | *Hongying Yang et al., Nutrient-Sensitive Mitochondrial NAD+ Levels Dictate Cell Survival, Cell, Vol 130, 1095-1107, 2007 |
| ・ | Joseph T. Rodgers, and Pere Puigserver, Fasting-dependent glucose and lipid
metabolic response through hepatic sirtuin 1, PNAS, 104(31): 12861-12866,
2007. http://www.pnas.org/cgi/content/abstract/104/31/12861 |
| ・ |
Zachary Gerhart-Hines, Joseph T Rodgers, Olivia Bare, Carles Lerin, Seung-Hee Kim1, , Raul Mostoslavsky, Metabolic control of muscle mitochondrial function and fatty acid oxidation through SIRT1/PGC-1 , The EMBO Journal (2007) 26, 1913-1923 http://www.nature.com/emboj/journal/v26/n7/abs/7601633a.html;jsessionid= 1BCDA1EA72624C2524F92CB34FDC927E |
| ・ | *Toren Finkel Manuel Serrano & Maria A. Blasco, The common biology of cancer and ageing, Nature 448:767-774, 2007. |
Sleep
最近、睡眠の短縮とMetabolic Syndromeとの関係を示唆する動物実験の結果が報告されるようになった(Turek05, Pearson06)。さらにこうした関係を示唆するものとして、核内受容体がcircadian rhythmに関係しているという報告がある。実際、circadian rhythmに関わる網羅的な遺伝子探索(Sato04, Ueda05、Duez08)によれば、Rev-erbαやR0Rαがその一部に含まれていることがわかっている。さらにPGC-1が哺乳類の時計とエネルギー代謝を関係づけているという報告もなされている(Liu07)。ハーステイグスらはHastingsらは、そうした調節を司るのが脳の視床下部にあるペースメーカー分子である、suprachiasmatic nuclei (SCN)だと報告している(Hastings07)。また、産総研の大石らは、フィブレート系の薬剤が、睡眠パターンを変化させるという現象を報告している。これらの報告から、肥満と睡眠障害とには因果関係が認められる、circadian rhythmは分子レベルと行動レベルでエネルギー代謝と関係している、睡眠障害とMetabolic Syndromeには相関がある、というような仮説を裏付ける証拠が揃いつつある(Laposky08)。Metabolic Syndromeが良質な睡眠を取ることで改善されるならば、生活様式によるMetabolic Syndrome対処法への新しい可能性が開かれることになる。
| ・ | John W. Shepard et al., History of the Development of Sleep Medicine in the United States, Journal of Clinical Sleep Medicine, 1(1): 61-82, 2005. |
| ・ | SPECIAL ARTICLES Fred W. Turek et al., Obesity and Metabolic Syndrome in Circadian Clock Mutant Mice, ScienceExpress, www.sciencexpress.org / 21 April 2005 / Page 1 / |
| ・ | Helen Pearson, SLEEP IT OFF, Nature 443: 261-263, 2006 |
| ・ | Trey K. Sato et al., Functional Genomics Strategy Reveals Rora as a Component of the Mammalian Circadian Clock, Neuron, 43(4): 527-537, 2004. |
| ・ | H. R. Ueda, et al., System-level identification of transcriptional circuits underlying mammalian circadian clocks, Nature Genetics, 37(2) : 187-192, 2005 |
| ・ | X. Yang et al., Nuclear Receptor Expression Links the Circadian Clock to Metabolism, Cell, 126: 801-810, 2006 |
| ・ | C. Liu et al., Transcriptional coactivator PGC-1 integrates the mammalian clock and energy metabolism、Nature, 447: 477-481, 2007. |
| ・ | M. Hastings, J.S. O'Neill and E. S. Maywood, Circadian clocks: regulators of endocrine and metabolic rhythms, Journal of Endocrinology, 195, 187-198, 2007. |
| ・ | R. Rintamaki et al., Seasonal Changes in Mood and Behavior Are Linked to Metabolic Syndrome, PLoS ONE. 3(1): e1482, 2008. |
| ・ | F. Levi & U. Schibler, Circadian rhythms: mechanisms and therapeutic implications. Annual Review of Pharmacology and Toxicology, 47: 593-628, 2007. |
| ・ | H. Duez, B. Staels, The nuclear receptors Rev-erbs and RORs integrate circadian rhythms and metabolism、Diabetes Vasc Dis Res 5:82-88, 2008; |
| ・ | **Aaron D. Laposky et al., Sleep and circadian rhythms: Key components in the regulation of energy metabolism, FEBS Letters, 582(1): 142-151 、2008. |
| ・ | **K. L. KNUTSON and E. VAN CAUTER, Associations between Sleep Loss and Increased Risk of Obesity and Diabetes, Annals of the New York Academy of Sciences、1129: 287 - 304, 2008. |
Metabolic Syndromeはヒトの生存に関する極めて根源的な事象にその原因があるように見える。そしてそのことは、ヒトという多細胞動物Metazoanの進化の系譜とも切り離せない。まず、Metabolic Syndromeは、物質とエネルギー代謝の収支バランスに関係している。ここから、ミトコンドリアを内部に抱えこんだ多細胞動物に共通する病態が生まれてくる。またそこでは、転写を介する物質代謝が重要な働きをしているが、それを担っている核内受容体は後生動物に固有のタンパク質であり、その構造と機能は後生動物に共通するところが大きい。ただし、人間の場合は、高度に発達した脳とそれが生み出した文明が健康の重要な環境因子となる。現代では、際限なく食物を求め、また、際限なく食欲をそそる料理法の進歩がある。それは、これまでの進化で形成されてきた脳による摂食制御系が機能不全に陥った状況とも解釈できる。このように、Metabolic Syndromeに陥る条件が整い過ぎている現代では、かつて成人病と言われた中高年で発症した各種の疾患が、若年層でも容易に発症する状況になっている。
年齢と共に発症率が上がってくる疾患が、Agingと関係あることは容易に推測されることであるが、いまや、この推測を裏付ける多くの遺伝子や経路網が明らかにされつつある。そうした遺伝子や経路網と、加齢に伴って発症する肥満、糖尿病、高血圧、高脂血症、動脈硬化、がん、さらにはアルツハイマー疾患のような神経変性症の関係を疑うのも自然な推測である。そしてその妥当性もいまや証明されつつある。
このような疾患へのリスクを軽減する最初の方策は、生活様式への配慮にある。分子生物学あるいはゲノム学を基礎とするMetabolic Syndrome研究の進歩は、これまでの食事や運動の効用をより正確に評価することを可能にするとともに、それらの実践法をより多彩なものにしている。さらに、食事と運動に加えて睡眠への注意も喚起している。
このように、Metabolic Syndromeの問題は、生物学の基礎的根源的な課題に関係しながら、日常生活における実践とも深く関係している課題である。医学の問題として今日的な意味をもつだけでなく、科学としても魅力のある分野だと言える。